
А. Ю. Леин
Институт океанологии им. П. П. Ширшова РАН (ИОРАН)
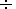 - 14,3 ) во флюидах и
нефтяных углеводородов в составе
сульфидных руд. Установлена изотопная неоднородность Сорг в сульфидных
рудах, подтверждающая его полигенную природу. Основной составляющей Сорг всех изученных руд является "свежая" и/или термически преобразованная
биомасса организмов гидротермального сообщества, живущих за счет процессов
хемосинтеза на Н2S, H2 и др. восстановленных соединениях гидротерм и
отличающихся от обычного фотосинтезированного Сорг. в океане или аномально
легким ( d13 С
- 14,3 ) во флюидах и
нефтяных углеводородов в составе
сульфидных руд. Установлена изотопная неоднородность Сорг в сульфидных
рудах, подтверждающая его полигенную природу. Основной составляющей Сорг всех изученных руд является "свежая" и/или термически преобразованная
биомасса организмов гидротермального сообщества, живущих за счет процессов
хемосинтеза на Н2S, H2 и др. восстановленных соединениях гидротерм и
отличающихся от обычного фотосинтезированного Сорг. в океане или аномально
легким ( d13 С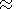 - 30 )
или аномально тяжелым
( d13 С
- 30 )
или аномально тяжелым
( d13 С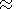 - 11 ) изотопным составом органического углерода.
Метан гидротермальных флюидов, в отличие от H2S и Н2, лишь частично
утилизируется микробным сообществом и поэтому должен составлять основную часть
пула растворенного СН4 в глубинных водах океана.
- 11 ) изотопным составом органического углерода.
Метан гидротермальных флюидов, в отличие от H2S и Н2, лишь частично
утилизируется микробным сообществом и поэтому должен составлять основную часть
пула растворенного СН4 в глубинных водах океана.
Изотопный состав серы и углерода - один из наиболее надежных и информативных показателей в геохимии гидротермального процесса, дающий представление о генезисе источника и о дальнейших путях преобразования соединений этих двух элементов на поверхности дна. Уже в первых работах [Arnold and Sheppard, 1981; Styrt et al., 1981], посвященных изучению изотопного состава серы гидротермальных сульфидных руд срединно-океанических хребтов (СОХ) было установлено, что сера рудообразующего раствора включает в себя серу из двух источников: (1) сульфидную серу из магматических пород ( d34 S=0,0 ) и (2) серу, образованную при восстановлении сульфата океанической воды ( d34 S-SO4 =20 ). Результаты изотопного анализа серы растворов и руд, а также результаты компьютерного моделирования дали основание считать, что причиной утяжеления изотопов гидротермальной серы относительно серы магматических сульфидов является увеличение доли изотопно-тяжелой серы, образующейся при восстановлении сульфат-иона океанической воды, на фоне постепенного уменьшения магматической серы в результате метасоматической преобразованности пород океанской коры [Гричук, Леин, 1991; Леин и др., 1991].
Другими словами, разнообразие наблюдаемых в растворах и рудах значений d34S сульфидов предлагалось объяснять разной степенью зрелости гидротермальных систем, подразделяя их на молодые "короткоживущие" и зрелые "долгоживущие" системы. Подразумевалось, что в недрах молодых систем сохраняется избыток неизмененных магматических пород (базальтов, долеритов), а в "зрелых" системах эти породы подвергаются длительной метасоматической проработке [Гричук, 1998].
Изотопный состав соединений углерода в сульфидных рудах и гидротермальных растворах СОХ и, в частности Срединно-Атлантического хребта (САХ) изучен несравненно менее детально, чем изотопный состав серных соединений. Источником соединений углерода в растворах предполагается СО, СО2 и СН4 магматических пород, суммарный( S CO2 = СО2 + НСО32- ) бикарбонат (растворенный органический углерод) морской воды.
Значения
d D ( d D=~100
) и
d13С-СН4 ( d13
С -15,0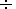 - 23,9,
[Chаrlou and Donval, 1993])
позволяют думать, что основная часть метана в гидротермальных растворах СОХ
образовалась в результате процесса Фишера-Тропша, т.е. в условиях
высокотемпературного синтеза (Т
- 23,9,
[Chаrlou and Donval, 1993])
позволяют думать, что основная часть метана в гидротермальных растворах СОХ
образовалась в результате процесса Фишера-Тропша, т.е. в условиях
высокотемпературного синтеза (Т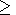 400oС) на водороде и СО:
400oС) на водороде и СО:
 CnH2n+2
+ nH2O
CnH2n+2
+ nH2O
 CnH2n+2
+ nCO2.
CnH2n+2
+ nCO2.
Все сказанное касается гидротермальных растворов и руд, формирующихся в базальтах MORB и долеритах предположительно над осевой внутрикоровой магматической камерой, в так называемой (I тип) осевой циркуляционной гидротермальной системе [Богданов и др., 1997].
В 1997 г. был открыт новый тип гидротермальной минералообразующей системы (II тип), получивший название глубинной циркуляционной системы, с реакционной зоной, расположенной на границе океанической коры и мантии в ультрабазитах и серпентинитах [Богданов и др., 1997]. Это открытие почти совпало по времени с обнаружением аномально высоких концентраций СН4 в придонных водах на значительном по длине отрезке (~2000 км) САХ от 12o с.ш. до 36o с.ш. [Bougault et al., 1998].
Присутствие СН4 во флюидах (27-301 мкМ/кг) является одной из характерных особенностей газового состава всех известных гидротермальных флюидов. Но в гидротермальных флюидах, образующихся при серпентинизации ультраосновных пород, концентрации СН4 достигают 2200 мкМ/кг [Donval et al, 1997], т.е. на 1-2 порядка превышают все известные ранее концентрации СН4 во флюидах осевой циркуляционной системы I типа.
Полученные новые данные по метановым аномалиям в придонных водах осевых
зон САХ и экстремально высокие концентрации СН4 во флюидах двух вновь
открытых активных гидротермальных полей 14o45 с.ш.
(Логачев) и 36o с.ш. (Рейнбоу), связанных с серпентинитовыми протрузиями,
вновь вызвали острый интерес к вопросу о происхождении СН4 и УВ флюидов,
в частности, в связи с проблемами нефтегазообразования. Этот факт нашел
отражение в ряде научных публикаций
[Дмитриев и др., 1999;
Дмитриевский и др., 1997].
с.ш.
(Логачев) и 36o с.ш. (Рейнбоу), связанных с серпентинитовыми протрузиями,
вновь вызвали острый интерес к вопросу о происхождении СН4 и УВ флюидов,
в частности, в связи с проблемами нефтегазообразования. Этот факт нашел
отражение в ряде научных публикаций
[Дмитриев и др., 1999;
Дмитриевский и др., 1997].
 Цель настоящей статьи - обобщение результатов исследования
изотопного
состава соединений серы и углерода в растворах, рудах и в биомассе
гидротермальных сообществ на гидротермальных полях разного возраста,
относящихся к двум разным типам гидротермальных систем, на примере 4-х
активных полей САХ 14o45
Цель настоящей статьи - обобщение результатов исследования
изотопного
состава соединений серы и углерода в растворах, рудах и в биомассе
гидротермальных сообществ на гидротермальных полях разного возраста,
относящихся к двум разным типам гидротермальных систем, на примере 4-х
активных полей САХ 14o45 ,
26o, 29o и 36o с.ш. САХ
(рис. 1,
табл. 1).
,
26o, 29o и 36o с.ш. САХ
(рис. 1,
табл. 1).
Первые данные по изотопному составу серы сульфидных руд, отобранных с поверхности ТАГ, показали существенное обогащение входящей в их состав серы тяжелым изотопом 34S [Леин и др., 1991, 1993]. В 1994 г. с помощью ГОА "Мир-1" и "Мир-2" была собрана и проанализирована более представительная коллекция сульфидных руд с поверхности рудного холма ТАГ (рис. 2а). Колебания значений d34S наблюдались в пределах от 2,2 до 11,2.
Изотопные исследования сульфидных руд и сульфидсодержащих пород, слагающих холм ТАГ, были проведены также на образцах, полученных при глубоководном бурении холма в 1995 г. [Gemmell and Sharpe, 1998]. Всего этими авторами было изучено 103 пробы. Средняя величина d34S сульфидной серы составила 7,2 при вариациях от 0,35 до 10,27.
Анализ материалов бурения показал, что длинная история гидротермальной активности ТАГ состоит из чередований высокотемпературных и холодных периодов. Для объяснения тяжелого изотопного состава сульфидной серы привлекается возможность проникновения холодной морской воды в рудное тело, в результате которого растворялись сульфатные минералы (гипс, ангидрит и др.), утяжеляя изотопный состав серы сульфидов на последующем восстановительном этапе жизни гидротермального холма. Следует заметить, что бурение проводилось на флангах, а не в центре холма, где возможно большее участие сульфата океанских вод в формировании рудного раствора по сравнению с центральной активной зоной, находящейся под влиянием горячего глубинного флюида.
Таким образом, анализ большого массива данных подтвердил выводы об аномально высоком содержании тяжелого изотопа серы в рудах гидротермальной системы ТАГ.
Проведено определение изотопного состава серы в образцах сульфидных руд (рис. 2б) и в Н2S из 2-х проб горячего флюида (табл. 1). Трубообразные постройки и шпилевидные сульфидные образования представлены преимущественно халькопирит-изокубанит-пирротин-ангидритовой минеральной ассоциацией. Массивные сульфиды с поверхности холмов и из основания труб состоят из пирита и сфалерита.
Исследования проб сульфидопроявления Брокен Спур показало различие не только в минеральных парагенезисах, но и в изотопном составе серы в рудах с поверхности холмообразных построек по сравнению с рудными трубами (chimneys). Пирит-сфалеритовые и сфалерит-пиритовые руды, слагающие поверхность холмов и основания труб, обеднены тяжелым изотопом по сравнению с изокубанит-халькопиритовой ассоциацией собственно трубообразных построек в среднем на 1. По изотопным и текстурно-структурным данным предполагается, что медьсодержащие сульфиды сформировались из более поздних растворов, в образовании Н2S которых принимала участие сера сульфат-иона морской воды, контактирующей с горячими базальтами.
Близкие значения d34S сульфидов приводятся для руд проявления Снейк Пит [Kase et al., 1990]. Имеющиеся данные по изотопному составу серы сульфидных руд из осевых гидротермальных циркуляционных систем I типа как будто бы в общих чертах подтверждают предложенную модель приуроченности изотопно-тяжелых руд к долгоживущим системам, а изотопно-легких - к молодым (рис. 2).
Гидротермальный флюид поля Логачев исследовался нами в 1998 г. в 41 рейсе НИС "Академик Мстислав Келдыш". Значения d34S серы растворенного H2S (табл. 1) и сульфидной взвеси варьировали от 2,2 до 2,8, т.е. были заметно обеднены изотопом 34S по сравнению с серой сульфидных руд, среднее значение d34 S которой равно 7,6 (рис. 2). Минеральные ассоциации и текстурно-структурные особенности руд детально описаны в работе Богданов и др. [1997]. Исследования выявили неоднородность изотопного состава серы сульфидных минералов. Авторы цитируемой работы говорят о двух противоположных тенденциях "в изменении соотношения изотопов серы в более поздних минералах: в сульфидах, кристаллизующихся на стенках канала, увеличивается доля легкого изотопа серы, а в сульфидах, замещающих ранние минералы или отлагающихся на внешних стенках постройки, повышается доля изотопно-тяжелой серы".
Наличие этих двух тенденций Богданов и др. [1997] объясняют двумя процессами. Во внешних зонах постройки обогащение серы сульфидов изотопом 34S вызвано участием в сульфидообразовании сульфат-иона океанской воды, а увеличение доли изотопно-легкой серы в сероводороде флюида и в наиболее поздних минеральных ассоциациях сульфидов может быть результатом вскипания минералообразующего флюида.
Итак, в процессе сепарации (вскипания) флюида изотопно-легкий сульфид ( d34 S = 2,2-2,8, табл. 1) может оставаться в растворе и достигать поверхности дна в составе горячего флюида, частично осаждаясь в порах и трещинах ( d34 S = 3,4, рис. 2в), а изотопно-тяжелые сульфиды осаждаются в подповерхностных условиях, возможно, образуя там штокверковые и жильные рудные тела.
Исследование поля Рейнбоу проводилось нами осенью 1998 и 1999 гг., в 41, 42 рейсах НИС "Академик Мстислав Келдыш". Рудный материал в коллекции представлен фрагментами неактивных и активных труб и массивными сульфидами из тел самих построек (свалы руд). Руды из отдельно стоящих курильщиков состоят из сульфидов Fe, Cu, Zn, часто с преобладанием цинковой минерализации. Руды из внешней зоны гидротермальных холмов имеют преимущественно медную специализацию. Во всех рудах присутствуют сульфиды железа - пирротин, пирит или марказит. По данным рентгенофлуоресцентного анализа в типичной сфалеритовой руде содержание Zn составляет около 30%, Cu~8%, Fe~18%, S~20%, Co~0,4%. В типичной медной руде - Zn~1,6%, Cu~22%, Fe~45%, S~22%, Co~0,9%. Среди основных минеральных фаз следует отметить высокотемпературный кубанит, содержащий 1,3% Со, несколько генераций сфалерита, в том числе его железистые разности (до 18% Fe), а также пирротин и пирит. Выделены три основные парагенные минеральные ассоциации: ранняя - пиритовая, главная - пирротин-пирит-сфалерит-халькопиритовая (кубанитовая) и поздняя - марказит(?)-пирит-халькопирит(+ борнит и ковеллин)- Fe-сфалеритовая.
Значения d34S сульфидной серы колеблются в пределах от 0,5 до 12,2. Наиболее поздние минералы - относительно крупные кристаллы (1-3 мм) халькопирита из центрального канала средней части трубы и тонкодисперсный железистый сфалерит из верхней части трубы - обеднены тяжелым изотопом 34S и имеют значения d34 S соответственно 0,5 и 0,6 (рис. 2г).
Значения d34 S растворенного сероводорода исследованных нами горячих флюидов поля Рейнбоу изменяются от 2,4 до 3,1 (табл. 1). С помощью приборов, установленныых на ГОА "Мир-1", на поле Рейнбоу, так же как на поле Логачев, наблюдалось пульсационное чередование выходящих на поверхность высокосоленых и опресненных разнотемпературных (Тo = 220-360o) флюидов. Это свидетельствует в пользу явления подповерхностной фазовой сепарации гидротермального раствора, приводящей, так же как на поле Логачев, к фракционированию химических элементов и их изотопов.
Анализ приведенных данных показал, что пределы вариаций значений
d34 S
cеры современных полиметаллических гидротермальных сульфидных руд в океане
(0,3
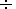 12,2 ) совпадают практически с пределами значений
d34S
серы древних полиметаллических залежей на континентах
[Krouse and Grinenko, 1991].
Средний изотопный состав серы гидротермальных руд континентов оценивается этими
авторами величиной ~3,5, средний изотопный состав серы гидротермальных
руд четырех активных полей САХ составил 4.
12,2 ) совпадают практически с пределами значений
d34S
серы древних полиметаллических залежей на континентах
[Krouse and Grinenko, 1991].
Средний изотопный состав серы гидротермальных руд континентов оценивается этими
авторами величиной ~3,5, средний изотопный состав серы гидротермальных
руд четырех активных полей САХ составил 4.
Выходящий на поверхность дна H2S гидротермальных флюидов и его производные (So, тиосульфаты) являются основным субстратом для процесса бактериального синтеза ОВ - процесса хемосинтеза. Вовлечение минеральных соединений серы микроорганизмами в процессы синтеза органических соединений является крупномасштабным биогеохимическим процессом глобального цикла серы.
Изотопные данные подтвердили, что окисление H2S флюида осуществляется
различными хемоавтотрофными микроорганизмами: свободными,
прикрепленными (обрастания, маты) и бактериями-симбионтами
[Леин и др., 1988;
Vetter and Fry, 1998].
Все измерения изотопного состава серы биомассы различных организмов гидротермальных
сообществ САХ имеют близкие пределы значений
d34 S =
- 0,7
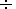 +3,7
(табл. 2).
Эти данные, во-первых, свидетельствуют о сравнительно гомогенном и
легком изотопном составе H2S флюидов и, во-вторых, говорят об отсутствии
сколько-нибудь заметного фракционирования при бактериальном окислении
восстановленных соединений.
+3,7
(табл. 2).
Эти данные, во-первых, свидетельствуют о сравнительно гомогенном и
легком изотопном составе H2S флюидов и, во-вторых, говорят об отсутствии
сколько-нибудь заметного фракционирования при бактериальном окислении
восстановленных соединений.
Симбиотрофные животные имеют практически такой же изотопный состав серы, что и хемоавтотрофные бактерии, заключенные в их специализированных тканях, т.е. наследуют изотопный состав исходных восстановленных соединений из флюидов.
Это позволяет использовать данные по сере биомассы симбиотрофных животных для установления источника восстановленной серы и ее изотопного состава, т.е. отличать организмы, живущие за счет продукции хемосинтеза от обычных морских животных, использующих фотосинтезированное ОВ, в том числе в древних гидротермальных постройках.
Гидротермальный флюид. Концентрация СН4 в горячих растворах САХ изменяется от 65 до 2310 мкМ (табл. 1). Минимальные концентрации СН4, наряду с самым высоким отношением Н2/СН4, характерны для флюида молодого поля Брокен Спур. Возможно, что на начальных этапах формирования гидротермальной системы поступление в нее бикарбоната (и растворенного Сорг ) с морской водой было ограничено. В этом случае синтез СН4 происходит сравнительно медленно, с заметным разделением изотопов углерода ( d13 С-СН4 = - 18,0, табл. 1). При этом большая часть Н2 не утилизируется и остается в растворе.
В долгоживущей гидротермальной системе ТАГ, напротив, отношение Н2/СН4 во флюиде указывает на почти равное содержание Н2 и СН4 в растворе, что говорит о достаточном количестве углерода, поступающего с морской водой, и об активном процессе метаногенеза, с меньшим, чем на Брокен Спур, разделением изотопов углерода СН4 ( d13 С-СН4 = - 14,6, табл. 1).
Во флюидах активных полей Логачев и Рейнбоу отношение Н2/СН4 составляет соответственно 5,4 и 5,9, что также свидетельствует об ограниченном количестве углерода при синтезе метана в этих двух гидротермальных системах и о неполной утилизации Н2 в процессе метаногенеза. Как уже упоминалось, происхождение метана во флюидах Логачев и Рейнбоу, в отличие от всех ранее известных полей, связано с серпентинизацией ультрабазитов по известной реакции:
|
6[(Mg1,5Fe0,5SiO4
+ 7H2O оливин | = |
3[Mg3Si2O5(OH)4]
+ серпентин |
Fe2O3 + H2, магнетит |
и с последующим образованием СН4 при взаимодействии водорода и растворенного бикарбоната морской воды;
 СН4 + 2Н2О .
СН4 + 2Н2О .
 Углерод метана ( d13 С-СН4 =
- 13,4
Углерод метана ( d13 С-СН4 =
- 13,4
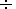 - 14,3 ) и СО2, остаточной
от процесса метаногенеза ( d13С-СО2 = 1
- 14,3 ) и СО2, остаточной
от процесса метаногенеза ( d13С-СО2 = 1
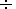 - 4,3
), во флюиде
Рейнбоу обогащен тяжелым изотопом соответственно на 1-10
и на 1-5
сравнительно
со всеми известными значениями углерода во флюидах других районов океана
(табл. 1,
рис. 3).
Скорее всего, это объясняется высокой скоростью процесса метаногенеза
в присутствии Ni-Fe катализатора при серпентинизации ультрабазитов
[Horita and Berndt, 1999].
- 4,3
), во флюиде
Рейнбоу обогащен тяжелым изотопом соответственно на 1-10
и на 1-5
сравнительно
со всеми известными значениями углерода во флюидах других районов океана
(табл. 1,
рис. 3).
Скорее всего, это объясняется высокой скоростью процесса метаногенеза
в присутствии Ni-Fe катализатора при серпентинизации ультрабазитов
[Horita and Berndt, 1999].
Измерение изотопного состава Сорг в сульфидных рудах показало, что значения d13 С варьируют от - 21,4 до - 27,9 (табл. 3), составляя в среднем - 24,7. Разброс изотопных данных свидетельствует о нескольких генетически неоднородных источниках Сорг в рудах.
Проблема происхождения органического вещества в гидротермальных
сульфидных рудах представляет интерес с точки зрения возможного абиогенного
синтеза СН4 и УВ в гидротермальных системах. Очевидно, что часть
органического вещества руд имеет биогенное происхождение, связанное как с
нормальным седиментационным осаждением Сорг на дно из фотической зоны, так
и с бактериальными процессами хемосинтеза и метанотрофии, протекающими на
активных гидротермальных полях дна океана на глубинах более 2-х км и достигает
менее 1% от величины первичной продукции фотосинтеза. Содержание Сорг в
отложениях пелагиали океана составляет
< 0,5%, а чаще всего 0,05-0,1%. В то
же время, в отложениях активных гидротермальных полей даже на глубине 3700 м
(ТАГ) содержание Сорг может возрастать до 1-2%
[Леин и др., 1998].
Значения
d13 С-С
орг. отложений океанского дна ( - 21,0
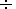 - 23,0 )
изотопно тяжелее средних значений
d13 С-Сорг гидротермальных
сульфидных руд. Предполагается, что рост содержания Сорг в гидротермальных
отложениях обязан, главным образом, продукции бактериального синтеза. Биомасса
бактерий-хемоавтотрофов и метанотрофов, продуцирующих ОВ на активных
гидротермальных полях, может существенно различаться по изотопному составу
углерода. Так,
d13 С-Сорг
биомассы свободно-живущих бактерий в водной
толще
над выходами флюидов изменяются от
- 22,6 до
- 27,5
(табл. 4), в то время
как
d13 С-Сорг биомассы прикрепленных "бентосных" бактерий,
живущих на твердом субстрате в виде бактериальных обрастаний или матов,
изотопно-тяжелее (табл. 5,
d13
С =
- 8,6
- 23,0 )
изотопно тяжелее средних значений
d13 С-Сорг гидротермальных
сульфидных руд. Предполагается, что рост содержания Сорг в гидротермальных
отложениях обязан, главным образом, продукции бактериального синтеза. Биомасса
бактерий-хемоавтотрофов и метанотрофов, продуцирующих ОВ на активных
гидротермальных полях, может существенно различаться по изотопному составу
углерода. Так,
d13 С-Сорг
биомассы свободно-живущих бактерий в водной
толще
над выходами флюидов изменяются от
- 22,6 до
- 27,5
(табл. 4), в то время
как
d13 С-Сорг биомассы прикрепленных "бентосных" бактерий,
живущих на твердом субстрате в виде бактериальных обрастаний или матов,
изотопно-тяжелее (табл. 5,
d13
С =
- 8,6
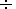 - 22,0 ). Легкий
изотопный состав органического углерода бактерий из водной толщи (табл. 4)
отражает очень медленный процесс синтеза ОВ при отсутствии лимита по СО2,
растворенной в воде. "Бентосные" бактерии, напротив, могут оказываться в
условиях лимита по СО2 при очень активном процессе окисления эндогенных
восстановленных соединений гидротермального флюида. Доля участия биомассы этих
2-х групп продуцентов в формировании изотопного состава Сорг руд
может быть различной.
- 22,0 ). Легкий
изотопный состав органического углерода бактерий из водной толщи (табл. 4)
отражает очень медленный процесс синтеза ОВ при отсутствии лимита по СО2,
растворенной в воде. "Бентосные" бактерии, напротив, могут оказываться в
условиях лимита по СО2 при очень активном процессе окисления эндогенных
восстановленных соединений гидротермального флюида. Доля участия биомассы этих
2-х групп продуцентов в формировании изотопного состава Сорг руд
может быть различной.
В рудах широко распространены остатки животных гидротермального сообщества. Следовательно, в сульфидных постройках наряду с микробной биомассой может захороняться биомасса животных, в основании пищевых цепей которых лежит также бактериальная продукция хемосинтеза и метанотрофии.
Основная масса биологического сообщества гидротермальных полей представлена эндо- или экзосимбиотрофными животными. Имеется обширная литература, из которой следует, что биомасса животных гидротермальных сообществ или обогащена тяжелым изотопом (группа животных с d13 Сорг = - 11,0 ), или обеднена им (группа животных с d13 Сорг = - 30,0 ) относительно углерода глубоководных морских организмов САХ (табл. 6).
Изотопный анализ С орг жирных кислот (липидов), выделенных из сульфидных руд САХ, изменяется от - 19,0 до - 23,0 (табл. 7). Значения d13 С углерода жирных кислот из биомассы бактерий-эпибионтов креветок Rimicaris exoculata, доминирующих в гидротермальных сообществах САХ, изменяется от - 12,0 до - 13,0 [Rieley et al., 1996]. Значения d13 С углерода индивидуальных жирных кислот из биомассы этих же креветок варьирует от - 11,0 до - 11,4 (табл. 7).
Приведенные данные по изотопии безусловно биогенного углерода биомассы бактерий и животных, в том числе углерода, входящего в состав жирных кислот, не объясняют обеднение изотопом 13С общего Сорг сульфидных руд САХ. Следовательно, можно предположить, что в рудах присутствует С орг иного происхождения, например, абиогенно синтезированные УВ.
Хромато-масс-спектрометрические исследования жирных кислот из сульфидных руд Брокен Спур и Логачев в сочетании с масс-фрагментографическим анализом показали заметную разницу в их составе, в частности, высокое содержание сложных многоатомных нефтеподобных н-алканов в рудах Логачев и Рейнбоу, не связанных напрямую с биогенным синтезом [Богданов и др., 1999; Леин и др., 1998; Пересыпкин и др., 1999]. В рудах Брокен Спур молекулярный состав н-алканов представлен в основном биогенными липидами (С16- С19, С25 ).
Изотопный состав углерода нефтяных углеводородов сульфидных руд не однороден и изменяется от - 24,7 до - 31,2 (табл. 8). Среднее значение d13 С= - 27,5.
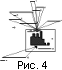 Таким образом, комплекс проведенных биохимических, изотопных,
биогеохимических и хроматографических исследований позволяет говорить о
сложной полигенной природе органических соединений в сульфидных рудах
(рис. 4)
и о большем вкладе предположительно абиогенно синтезированных
н-алканов в состав С орг гидротермальных руд, вмещающими породами
которых являются серпентиниты.
Таким образом, комплекс проведенных биохимических, изотопных,
биогеохимических и хроматографических исследований позволяет говорить о
сложной полигенной природе органических соединений в сульфидных рудах
(рис. 4)
и о большем вкладе предположительно абиогенно синтезированных
н-алканов в состав С орг гидротермальных руд, вмещающими породами
которых являются серпентиниты.
Есть основание считать, что синтез СН4 и углеводородов в гидротермальных
системах САХ идет по-разному. В осевой циркуляционной гидротермальной
системе ТАГ и Брокен Спур основная часть метана флюидов образуется в
результате процесса Фишера-Тропша с заметным разделением изотопов
углерода
d13ССН4 =
- 14,6
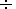 - 18,0 ).
В глубинной
циркуляционной системе процесс метаногенеза происходит при взаимодействии
водорода, образованного при серпентинизации ультрабазитов, с бикарбонатом
океанской воды, в присутствии активного Ni-Fe катализатора, который убыстряет
процесс синтеза СН4, и тем самым препятствует значительному фракционированию
изотопов углерода СН4 по сравнению с углеродом исходного бикарбоната
( d13 С =
- 13,4
- 18,0 ).
В глубинной
циркуляционной системе процесс метаногенеза происходит при взаимодействии
водорода, образованного при серпентинизации ультрабазитов, с бикарбонатом
океанской воды, в присутствии активного Ni-Fe катализатора, который убыстряет
процесс синтеза СН4, и тем самым препятствует значительному фракционированию
изотопов углерода СН4 по сравнению с углеродом исходного бикарбоната
( d13 С =
- 13,4
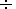 - 14,3, табл. 1).
Наличие в сфере реакций
СН4, свободного водорода, СО2, воды и металлов - катализаторов синтеза
может приводить к образованию сложных молекул углеводородов и их производных,
например, по реакции:
- 14,3, табл. 1).
Наличие в сфере реакций
СН4, свободного водорода, СО2, воды и металлов - катализаторов синтеза
может приводить к образованию сложных молекул углеводородов и их производных,
например, по реакции:
 С2Н5ОН + Н2О .
С2Н5ОН + Н2О .
По расчетам О. Г. Сорохтина
[Сорохтин, Ушаков, 1991]
в рифтовых зонах океана в течение года может образовываться 1800
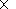 106 т
серпентинитов и соответственно 32
106 т
серпентинитов и соответственно 32
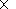 106 т СН4. Результаты моделирования
взаимодействия морской воды с толеитовыми базальтами и гарцбургитом также
свидетельствуют о возможной генерации большого количества Н2 и СН4.
Так, при серпентинизации 1 км
3 гарцбургита может образоваться
5
106 т СН4. Результаты моделирования
взаимодействия морской воды с толеитовыми базальтами и гарцбургитом также
свидетельствуют о возможной генерации большого количества Н2 и СН4.
Так, при серпентинизации 1 км
3 гарцбургита может образоваться
5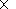 105 т
Н2 и 2,5
105 т
Н2 и 2,5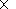 105 т
СН4 [Дмитриев и др., 1999].
Часть этих абиогенно синтезированных Н2 и СН4
вместе с Н2S выходят в
составе флюидов на поверхность дна, где используются в процессах
бактериального хемосинтеза и метанотрофии. Образующаяся при этом биомасса
микроорганизмов отличается по изотопному составу серы и углерода от
фотосинтезированного ОВ.
105 т
СН4 [Дмитриев и др., 1999].
Часть этих абиогенно синтезированных Н2 и СН4
вместе с Н2S выходят в
составе флюидов на поверхность дна, где используются в процессах
бактериального хемосинтеза и метанотрофии. Образующаяся при этом биомасса
микроорганизмов отличается по изотопному составу серы и углерода от
фотосинтезированного ОВ.
Сероводород и водород флюидов безусловно полностью утилизируются микрофлорой на активных полях. Этого нельзя сказать с уверенностью о метане, поскольку наблюдаются аномальные концентрации СН 4 в придонных слоях воды на огромных площадях далеко от мест истечения флюидов [Charlou et al., 1998]. Добавим, что СН4 - очень устойчивое соединение и его окисление в биосферных условиях возможно только при участии специфических групп метанокисляющих микроорганизмов. Экспериментальные определения скорости бактериального окисления СН4 в отложениях дна и в водной толще дают, как правило, очень низкие оценки скорости этого процесса [Гальченко и др., 1989; Леин и др., 1993], подтверждая тот факт, что только небольшая часть СН4 гидротермальных флюидов утилизируется метанотрофами, а основная его часть разносится течениями и рассеивается в океане. Следовательно, в водной толще океана, наряду с биогенным, должно присутствовать значительное количество абиогенно синтезированного гидротермального изотопно-тяжелого СН4. По различным оценкам при бактериальных процессах окисления Н2S, Н2 и других восстановленных соединений на активных гидротермальных полях продуцируется около 1% от общего Сорг, образующегося в фотослое океана, и около 50% в среднем от количества Сорг, достигающего дна в рифтовых зонах.
В составе Сорг гидротермальных образований, наряду с бесспорно биогенными липидами, присутствуют сложные многоатомные н-алканы, состав которых не связан напрямую с преобразованием биогенных структур. Содержание таких н-алканов значительно выше в сульфидных рудах из серпентинитовых вмещающих пород. Но и в этих гидротермальных образованиях количество нефтяных углеводородов резко превышает 10% от общего количества Сорг, поэтому пока нет оснований рассматривать абиогенный синтез УВ как существенный источник нефтяных УВ в океане.
Богданов Ю. А., Лисицын А. П., Муравьев К. Г. и др., Общие закономерности формирования гидротермальных образований, Кн.: Гидротермальные образования Срединного хребта Атлантического океана, Ред. А. П. Лисицын, с. 172-190, Наука, Москва, 1992.
Богданов Ю. А., Бортников Н. С., Викентьев И. В. и др., Новый тип современной
минерализующей системы: "черные курильщики" гидротермального поля 14o45
 с.ш.,
Срединно-Атлантический хребет, Геология рудных месторождений, 39, (1), 68-90,
1997.
с.ш.,
Срединно-Атлантический хребет, Геология рудных месторождений, 39, (1), 68-90,
1997.
Богданов Ю. А., Сагалевич А. М., Гурвич Е. Г. и др., Подводные геологические исследования гидротермального поля Рейнбоу (Срединно-Атлантический хребет), Доклады РАН, 365, (5), 657-662. 1999.
Гальченко В. Ф., Леин А. Ю., Иванов М. В., Микробиологические и биогеохимические процессы в водной толще океана как показатель активности подводных гидротерм, Геохимия, (8), 1075-1088, 1989.
Гричук Д. В., Термодинамические модели субмаринных гидротермальных систем, Автореф. дис. на соискание учен.ст. д.г.-м.н., с. 57, Москва, 1998.
Гричук Д. В., Леин А. Ю., Эволюция океанской гидротермальной системы и изотопный состав серы сульфидов, ДАН СССР, 318, (2), 422-425, 1991.
Дмитриев Л. В., Базылев Б. А., Борисов М. В. и др., Образование водорода и метана при серпентинизации мантийных гипербазитов океана и происхождение нефти, Российский журнал наук о Земле, 1, (6), 511-519, 1999.
Дмитриевский А. Н., Каракин А. В., Баланюк И. Е., Матвеенков В. В., Гидротермальный механизм образования углеводородов в срединно-океанических хребтах, Геология нефти и газа, (8), 4-16, 1997.
Леин А. Ю., Гальченко В. Ф., Павлова Г. А., Пименов Н. В., Биогеохимические процессы в районе активного гидротермального поля в рифтовой зоне ТАГ, Кн.: Гидротермальные системы и осадочные формации срединно-океанических хребтов Атлантики, Ред. Лисицын А. П., с. 113-146, Наука, Москва, 1993.
Леин А. Ю., Гальченко В. Ф., Гриненко В. А. и др., Минеральный состав и геохимия пород с бактериальными обрастаниями из подводных гидротермальных построек, Геохимия, (9), 1235-1248, 1988.
Леин А. Ю., Ульянова Н. В., Гриненко В. А., Лисицын А. П., Геохимические особенности сульфидных руд Срединно-Атлантического хребта (26o с.ш.), Геохимия, (3), 307-319, 1991.
Леин А. Ю., Гальченко В. Ф., Пименов Н. В., Иванов М. В., Роль процессов бактериального хемосинтеза и метанотрофии в биогеохимии океана, Геохимия, (2), 252-268, 1993.
Леин А. Ю., Галкин С. В., Гебрук А. В., Миллер Ю. М., Пименов Н. В., Москалев Л. И., академик Иванов М. В., Роль бактериального хемосинтеза в питании сообщества животных активного гидротермального поля Брокен Спур, Доклады РАН, 357, (3), 410-413, 1997.
Леин А. Ю., Глущенко Н. Н., Ульянова Н. В., академик Иванов М. В., Биомаркеры сульфидных руд современных и древних "черных курильщиков", Доклады РАН, 359, (4), 525-528, 1998.
Пересыпкин В. И., Леин А. Ю., Богданов Ю. А., Бортников Н. С.,
Липиды в
гидротермальных образованиях в районе 14o45
 с.ш. и 29o с.ш.
САХ, Океанология, 39, (2), 258-269, 1999.
с.ш. и 29o с.ш.
САХ, Океанология, 39, (2), 258-269, 1999.
Пименов Н. В., Саввичев А. С., Гебрук А. В. и др., Трофическая специализация креветок-брезилиид в гидротермальном сообществе ТАГ, Докл. РАН, 323, (3), 776-781, 1992.
Сорохтин О. Г., Ушаков С. А., Глобальная эволюция Земли, с. 446, Изд. МГУ, Москва, 1991.
Arnold M. and Sheppard S. M. F., East Pacific Rise at latitude 21o N: Isotopic composition and origin of the hydrothermal sulfur, Earth and Planet. Sci. Lett., 56, (1), 149-156, 1981.
Bougault H., Aballea M., Radford-Knoery J. et al., FAMOUS and AMAR segments on the Mid-Atlantic Ridge: Ubiquitous hydrothermaL Mn, CH 4 , d3 He signals along the rift valley walls and rift offsets, Earth and Planet. Sci. Lett., 161, 1-17, 1998.
Charlou J. L. and Donval J. P., Hydrothermal methane venting between 12oN and 26oN along the Mid-Atlantic Ridge, J. Geophys. Res., 98, (B6), 9625-9642, 1993.
Charlou J. L., Fouquet Y., Bougault H. et al., Intense CH4 plumes generated
by serpentinization of ultramafic rocks at the intersection of the
15o20 N
fracture zone and the Mid-Atlantic Ridge, Geochim. et Cosmochim. Acta, 62,
(13), 2323-2333, 1998.
N
fracture zone and the Mid-Atlantic Ridge, Geochim. et Cosmochim. Acta, 62,
(13), 2323-2333, 1998.
Donval J. P., Charlou J. L., Douville T. et al., High H2 and CH4 content
in hydrothermal fluids from Rainbow site newly sampled at
36o14 N
on the Amar segment, Mid-Atlantic Ridge (Diving FLORES cruise, July 1997),
Comparison with other MAR sites, EOS TRANS, 78, F 832, 1997 (abstr.).
N
on the Amar segment, Mid-Atlantic Ridge (Diving FLORES cruise, July 1997),
Comparison with other MAR sites, EOS TRANS, 78, F 832, 1997 (abstr.).
Duckworth R. C., Knott R. and Fallick A. E., Mineralogy and sulphur isotope geochemistry of the Broken Spur sulphides, 29o N, Mid-Atlantic Ridge, Hydrothermal vents and processes, London, Geol. Soc. Spec. Publ., (87), 175-190, 1995.
Gemmel J. B. and Sharpe R., Detailed sulfur isotope investigation of the TAG hydrothermal mound and stockwork zone, 26o N, Mid-Atlantic Ridge, Proc. ODP. Sci. Results, 158, Herzig P. et al. (Eds.), 1998.
Horita J. and Berndt M. E., Abiogenic methane formation and isotopic fractionation under hydrothermal conditions, Science, 285, (5430), 1055-1058, 1999.
James R. H., Elderfield H. and Palmer M. R., The chemistry of hydrothermal fluids from the Broken Spur site, 29o N Mid-Atlantic Ridge, Geochem. et Cosmohim. Acta, 59, (4), 651-659, 1995.
Kase K., Yamamoto M. and Shibato T., Copper-rich sulfide deposit near 23o N, Mid-Atlantic Ridge: chemical composition, mineral chemistry, and sulfur isotops, Proc. ODP, Leg 106/109, Sci. Results, 163-177, 1990.
Krouse H. R. and Grinenko V. A. (Eds), Stable isotopes natural and antropogenic sulphur in the environment, SCOPE 43, 440, 1991.
Polz M. F., Robinson J. J., Cavanaugh C. M. and Van Dover C. L., Trophic ecology of massive shrimp aggregations at Mid-Atlantic Ridge hydrothermal vent site, Limnol. Oceanogr., 43, (7), 1631-1638, 1998.
Pond D. W., Bell M. V., Dixon D. R. et. al., Stable-carbon-isotope composition of fatty acids in hydrothermal vent mussels containing methanotrophic and thiotrophic bacterial endosymbionts, Applied and Enviroumental Microbiolog., 64, 370-375, 1998.
Rieley G., Van Dover C. L., Hedrick D. and Eglinton G., Trophic ecology of Remicaris exoculata from TAG as revealed by relative abundance and isotopic composition of individual fatty acids, Conference Abstracts, (1), 846-847, 1996.
Styrt M. M., Brockman A. J., Holland H. D. et al., The mineralogy and the isotopic composition of sulfur in hydrothermal sulfide/sulfate deposit in the East Pacific Rise, 21o N latitude, Earth and Panet. Sci. Lett., 53, (3), 382-390, 1981.
Trusk J. H. and Van Dover C. L., Site-specific and ontogenetic variations in nutrition of mussels (Bathymodiolus sp.) from the Lucky Strike hydrothermal vent field, Mid-Atlantic Ridge, Limnol. Oceanogr., 44, (2), 334-343, 1999.
Van Dover C. L., Ecology of Mid-Atlantic Ridge hydrothermal vents, Hydrothermal vents and processes, 87, (Eds. Parson L. M., Walker C. L., Dixon D. R.), pp. 257-294, Geological Society Special Publication, 1995.
Van Dover C. L., Desbruyeres D., Segonzac M. et al., Biology of the Lucky Strike hydrothermal field, Deep-Sea Res. I, 43, (9), 1509-1529, 1996.
Vereshchaka A. L., Vinogradov G. M., Lein A. Yu. et al., Carbon and nitrogen isotopic composition of the fauna from the Broken Spur hydrothermal vent, Mar. Biol., 136, (1), 11-17, 2000.
Vetter R. D. and Fry B., Sulfure contentes and sulfur isotope compositions of theotrophic symbioses in bivalve mollusks and vestimentiferan worms, Mar. Biol., 132, 453-460, 1998.
 |